- 目 次
-
This Week at NEJM.org
NEJM.orgからピックアップされている注目記事の一覧です.
October 31, 2002
Vol. 347 No. 18
-
心不全の発生率と生存率の動向
Trends in the Incidence of and Survival with Heart Failure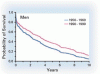
うっ血性心不全は予後が非常に不良である.このフラミンガム心臓研究(Framingham Heart Study)からの調査では,心不全の発生率と発症後の生存率に関する 50 年間の動向を追跡した.この期間中,心不全の発生率は女性では低下したが男性では低下しなかった.一方,生存率は男女共に改善された.
研究期間中にかなり改善されたにもかかわらず,心不全患者の 5 年生存率は依然として 50%程度のままである.このことは,この重篤な健康問題を予防するよりよい方法が緊要であることを示している. -
ジゴキシン治療を受けた心不全女性における死亡率の上昇
Increased Mortality among Women with Heart Failure Treated with Digoxin
ジギタリス研究グループは,ジゴキシン投与を受けた心不全患者とプラセボ投与患者間に死亡率の差がないことを報告した.今回の事後解析では,試験に参加した男性と女性を別々に解析した.ジゴキシン療法は,男性では死亡率に影響を及ぼさなかったが,女性では全死亡率の上昇と関連していた(ジゴキシン群 33.1%,プラセボ群 28.9%).
この知見は事後解析によって得られたものであるが,女性の心不全治療に対するジゴキシンの使用について,重要な疑問を提起し,再調査を要求している. -
壊疽性膿皮症と誤診された皮膚潰瘍
Skin Ulcers Misdiagnosed as Pyoderma Gangrenosum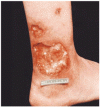
壊疽性膿皮症と皮膚潰瘍の他の原因を見分けるのはむずかしいことがある.この研究では,著者らは壊疽性膿皮症に似た皮膚潰瘍患者 95 例を同定した.それらの潰瘍は,実際には,血管閉塞性疾患や静脈疾患,脈管炎,癌,感染症,薬剤誘発性または外因性の組織損傷,あるいは他の炎症性疾患が原因であった.壊疽性膿皮症と診断された患者のほとんどが治療され,治療を受けたうちの 36%には,基礎疾患の悪化あるいは診断の遅延がみられた.
壊疽性膿皮症は,除外診断である.壊疽性膿皮症が疑われる患者では,皮膚潰瘍の別の原因を評価することが重要である. -
Special Article:インドにおける結核対策
Special Article: Tuberculosis Control in India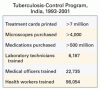
インドでは,毎年 50 万人近くの人が結核で死亡している.国家的結核対策プログラムの最近の改善により,治療法,追跡調査,および報告義務が標準化された.20 万人以上の新しい公衆衛生従事者が養成され,約 340 万人の患者が結核の検査を受けた.80 万人近くの患者が治療を受け,成功率は約 83%であった.費用は,患者 1 人の治療につき約 50 ドルである.
インドにおける結核対策プログラムは,世界最大の公衆衛生対策の 1 つである.国家プログラムはより有効となってきているが,まだ人口の半分以下にしか達していない.インドは世界の全結核症例の約 1/3 を占めているので,持続的な展開が重要である. -
最近の概念:心室中隔破裂
Current Concepts: Rupture of the Interventricular Septum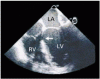
急性心筋梗塞に心室中隔破裂が合併した場合,死亡率は高く,緊急の手術介入が必要となる.この概説では,再灌流療法により中隔破裂の頻度は減少したが,迅速な診断が依然として必須であることを説明している.ドップラー心エコー検査は通常診断に有用であり,左右シャントの大きさの推定にも利用できる.
-
Health Policy Report:小児における薬物の評価
Health Policy Report: Testing Medications in Children小児に対する薬物の安全性と有効性の評価をさらに活発にするため,2 つの連邦規制が制定された.小児限定条項は,小児を対象とした薬物の評価を自発的に行う企業に対し,さらに 6 ヵ月の特許保護を与える.一方,小児規定は,薬剤が小児にとって重要な場合に小児試験を要求する.
臨床試験に組み入れられる小児は増加しつつある.長期的効果は,研究を倫理的かつ効果的に実施することと,小児における薬剤の安全性と有効性の評価に政府が継続的に関与することにかかっている.



